はじめに
子宮内膜の微生物組成は、生殖医療における診断・予後バイオマーカーとして注目されています。現在の子宮内膜マイクロバイオーム研究は主にDNAベースの16S rRNA遺伝子シーケンシングに基づいていますが、DNA検出は死菌や残存遊離DNAも増幅するため、生きた微生物の存在を意味するものではありません。メタトランスクリプトーム解析(RNAベース)は、実際に転写活性を持つ生きた微生物の機能的情報を捉えることができます。今回、同一女性から採取した検体に対してDNAおよびRNAベースの解析を並行して行い、女性生殖器系の微生物組成と機能的活性を包括的に比較した横断研究をご紹介いたします。
ポイント
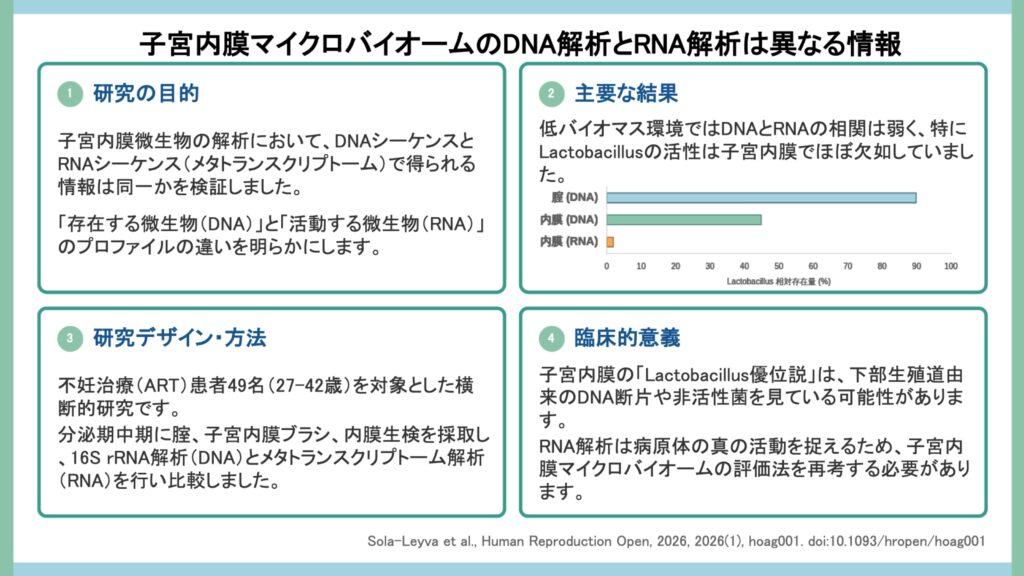
子宮内膜においてDNA解析とRNA解析の相関は弱く、Lactobacillusの転写活性は子宮内膜生検では検出されず、子宮内膜に存在するLactobacillus DNAは下部生殖管由来の残存DNAや非活動性細胞に由来する可能性が示唆されました。
引用文献
Sola-Leyva A, et al. Hum Reprod Open. 2026;2026(1):hoag001. doi: 10.1093/hropen/hoag001.
論文内容
子宮内膜微生物のDNAまたはRNAシーケンシングベースの解析手法が同一の情報を提供するかどうかを検討した横断研究です。対象はARTを受けている生殖年齢女性49名(27〜42歳)で、主コホート44名と検証コホート5名で構成されました。月経周期の分泌中期(LHサージ後6〜9日)に、腟スワブ、子宮内膜ブラシ、子宮内膜生検の各検体を採取しました。
本研究は2段階の解析設計です。主コホート(N=44)では、子宮内膜生検のみDNA(16S rRNA遺伝子シーケンシング)とRNA(メタトランスクリプトーム)の両方を実施し、腟スワブと子宮内膜ブラシはDNA解析のみとしました。この設計により、まず子宮内膜生検においてDNAで検出された微生物がRNAレベルでも転写活性を示すかどうかを検討しています。検証コホート(N=5)では、腟・ブラシ・生検の全3検体でDNA・RNA両方を実施し、さらに生検にはqPCRと培養も追加しました。検証コホートの目的は、主コホートで観察された子宮内膜のDNAとRNAの不一致が、サンプリング手順のアーティファクト(例えば、先にブラシで微生物を除去してしまったために生検でRNAが検出されなかった可能性)ではないことを確認することです。
DNAベース解析では16S rRNA遺伝子のV4領域を増幅しシーケンスしました。低バイオマス環境では実験試薬由来の微量な微生物DNAが検体中のシグナルと同程度になり得るため、in silicoコンタミネーション除去としてDecontam Rパッケージを用いました。
結果
腟マイクロバイオームは主にLactobacillusが優勢であり、VALENCIAアルゴリズムによるCST(Community State Type:腟マイクロバイオームの群集構造分類で、L. crispatus優位のCST I、L. gasseri優位のCST II、L. iners優位のCST III、L. jensenii優位のCST V、Lactobacillus非優位のCST IVの5型に分類)では80%がLactobacillus優位型、20%がdysbiosisに相当するCST IVに分類されました。子宮内膜のDNAベース解析では腟と比較してLactobacillusの割合が著しく低下し、より多様な細菌属が検出されました。一方、メタトランスクリプトーム解析(RNAベース)による子宮内膜生検ではStaphylococcus、Salmonella、Bacillus、Escherichia、Klebsiellaなどが検出されましたが、Lactobacillusは検出されませんでした。
α多様性(検体内の微生物多様性指標)では、子宮内膜のShannon多様性指数・種豊富度(richness)はいずれも腟より有意に高く(P < 0.0001)、子宮内膜生検ではRNA-seqの方が16Sより多様性が高い結果でした(P < 0.05)。β多様性(検体間の微生物群集の違い)では、すべてのグループ間で有意な非類似性が認められ(P < 0.001)、サンプリング方法と核酸の種類の両方が検出される微生物プロファイルに影響することが示されました。
検証コホートでは、腟の微生物リードが子宮内膜の約1000倍であることが定量的に示されました。重要なこととして、ブラシ採取を行わずに直接生検を採取した参加者でもLactobacillusのRNAは検出されず、主コホートの所見がサンプリングアーティファクトではないことが確認されました。RNA-seqは16S解析よりdysbiosis関連細菌(Gardnerella、Ureaplasma)の検出解像度が高く、16Sでは検出できなかったGardnerellaを子宮内膜で検出した唯一の手法でした。
種レベル同定では、16S解析で腟検体のL. helveticusと同定された菌が、RNA-seqではL. crispatus優位と判明しました。両者は姉妹種で16S V4領域では区別困難であり、種特異的qPCRではこの誤分類を回避できます。ただしqPCRもDNA標的であり死菌検出の制約は共通です。またNGSは相対評価のため低バイオマス環境でコンタミネーションが過大評価されるリスクがあり、qPCRの絶対定量はこの点で有利です。
子宮内膜ブラシ検体でDNA・RNA両方で有意な正の相関を示したのはFannyhessea、Gardnerella、Ureaplasmaの3種であり、これらの病原体はLactobacillusとは対照的に子宮内膜で転写活性を維持している可能性が示唆されました。腟では45菌中6種がDNA・RNA間で有意な正の相関を示したのに対し、子宮内膜生検では18菌中Tepidimonasの1種のみであり、子宮内膜ではDNA解析とRNA解析の乖離が大きいことが明確に示されました。
私見
最も重要な知見は、子宮内膜生検でLactobacillusの転写活性が検出されなかったことです。DNAベースの研究でLactobacillus優位(>90%)が高い妊娠率と関連するとの報告(Moreno I, et al. Microbiome. 2022)が広く知られていますが、そのDNAが生菌を反映しているのかという根本的な問いを本研究は提起しています。先行研究(Sola-Leyva A, et al. Hum Reprod. 2021)でも子宮内膜のLactobacillus存在量は1%未満と報告されており、今回の結果はこれを再現しています。検証コホートでブラシなしの直接生検でもLactobacillus RNAが検出されなかったことで、サンプリングアーティファクトの可能性が否定された点は特に重要です。
背景として、Lactobacillusは低pH環境(pH 3.5〜4.5)で増殖に適した細菌ですが、子宮内膜のpHは中性〜弱アルカリ性です(Parratt JR, et al. J Reprod Fertil. 1995; Lykke MR, et al. Pathogens. 2021)。このpH環境の不適合が転写活性欠如の一因と考えられます。一方、dysbiosis関連病原体(Gardnerella、Fannyhessea、Ureaplasma)はLactobacillusとは対照的にDNA・RNA両方で相関を示し、子宮内膜で転写活性を維持しうることが示唆されました。
方法論的には、子宮内膜マイクロバイオーム研究の課題は、①DNA検出が生菌を反映しない問題(全DNAベース手法に共通)、②相対評価による過大評価リスク(NGS固有)、③種レベル分類精度の限界(16S固有)の3層に分かれます。qPCRは②③を回避できますが①は共通であり、根本的解決にはRNAベース解析やPMA処理後のPCRが必要です。
限界として、子宮内膜の微生物リードは腟の約1000分の1と極めて少なく、Lactobacillusの転写活性が「存在しない」のか「検出限界以下」なのかは厳密に区別できません。
現在臨床で用いられている検査はいずれもDNAベースである点を意識して検査解釈をしていく必要がありそうです。
文責:川井清考(WFC group CEO)
お子さんを望んで妊活をされているご夫婦のためのコラムです。妊娠・タイミング法・人工授精・体外受精・顕微授精などに関して、当院の成績と論文を参考に掲載しています。内容が難しい部分もありますが、どうぞご容赦ください。当コラム内のテキスト、画像、グラフなどの無断転載・無断使用はご遠慮ください。

















